전체뉴스 71-80 / 26,829건
- 최신순
- 정확도순
- 과거순
-
카나프테라퓨틱스 “ADC 차별화된 완전 액상 제형 개발”
... 롯데바이오로직스 측은 “이 대표의 이력, 카나프테라퓨틱스가 내부적으로 개발 중인 ADC 플랫폼의 기술력을 높이 평가했다”고 설명했다. 이 대표는 2010~2016년 제넨텍에서 근무했다. 제넨텍은 미국 식품의약국(FDA) 품목허가를 받은 ADC 제품 13개 중 2개(캐싸일라, 폴리비)의 제품을 보유하고 있다. 그는 제넨텍에서 ADC 새로운 링커 약물(new linker drug, NLD) 개발, 넥스트 제너레이션(Next generation) 항HER2 ...
바이오인사이트 | 2024.04.29 09:27 | 김유림
-
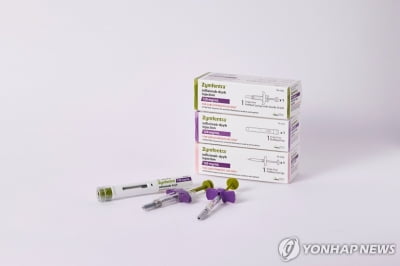
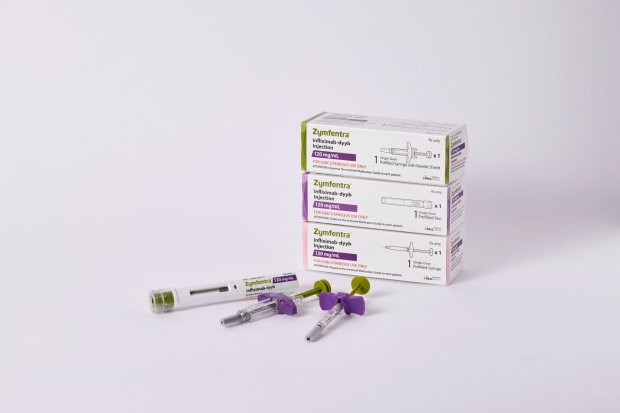
셀트리온 "짐펜트라, 美 3대 PBM 선호의약품 등재"
... 것으로 보고 있다. 짐펜트라는 기존 셀트리온의 정맥주사 제형 자가면역질환 치료제 바이오시밀러(바이오의약품 복제약)인 '램시마'(성분명 인플릭시맙)를 자가 투여가 가능한 피하주사 제형으로 변경해 개발한 제품으로, 지난해 10월 미국 식품의약청(FDA)으로부터 신약으로 허가받았다. 프랜신 갈란테 셀트리온 미국 법인 마켓 엑세스 총괄 책임자는 "이번 계약을 통해 미국에서 수백만 명의 만성질환자들이 치료 혜택을 받을 수 있는 중요한 변화의 길이 열렸다"며 "셀트리온은 만성질환으로 ...
한국경제 | 2024.04.29 09:09 | YONHAP
-
셀트리온 신약 짐펜트라, 3대 PBM 등재로 美서 판로 확보
... 차지하고 있다. 이번 계약과 더불어 이미 처방집 등재가 이뤄진 중소형 PBM을 포함할 경우, 짐펜트라는 미국 전체 사보험 시장에서 약 40%의 커버리지(가입자 수 기준)를 확보한 것으로 분석된다. 짐펜트라는 미국 식품의약국(FDA)으로부터 승인 받은 세계 유일의 인플릭시맙 SC 제형으로 현재 미국에서 판매되고 있다. 셀트리온은 짐펜트라를 비롯해 FDA에서 승인 받은 회사 제품들의 가치를 더욱 넓게 전달하기 위해 국가 및 지역 건강 플랜을 비롯해 PBM, ...
바이오인사이트 | 2024.04.29 08:49 | 안대규
-
셀트리온, 익스프레스 스크립츠와 짐펜트라 등재 계약 체결
... 계약을 통해 짐펜트라는 2,190만명의 커버리지를 보유한 ESI 처방집(Express Scripts National Preferred Formulary)에 선호의약품(preferred drug)으로 등재됐다. 짐펜트라는 미국 식품의약국(FDA)으로부터 승인 받은 세계 유일의 인플릭시맙 피하주사(SC) 제형으로 현재 미국에서 판매되고 있다. 셀트리온은 자가면역질환 치료제인 짐펜트라를 비롯해 FDA에서 승인 받은 회사 제품들의 가치를 더욱 넓게 전달하기 위해 국가 및 지역 건강 ...
한국경제 | 2024.04.29 08:12 | WISEPRESS
-
"카드로 코로나19 예방" 의대 교수 집유
... 교수는 당시 자신이 개발했다는 명함 크기의 카드를 책의 부록으로 제공하면서 "코로나19로부터 예방될 수 있고 확진자와 환자도 쉽게 회복될 수 있다", "2상 시험을 통해 효능은 충분히 입증됐다. 효과는 100%", "미국 식품의약국(FDA)에 일반의약품 등록이 돼 있다"고 광고했다. 이 카드가 "코로나19 치료제 혼합 용액의 파동을 디지털화해 출력한 것"이라며 특허 청구를 하기도 했다. 2021년 2월에는 서울 여의도순복음교회 예배에서 담임목사가 이 카드를 나눠주겠다며 ...
한국경제TV | 2024.04.29 07:29
-
"카드 한장이면 코로나19에 100% 효과" 의대 교수 징역형 집유
... 교수는 당시 자신이 개발했다는 명함 크기의 카드를 책의 부록으로 제공하면서 "코로나19로부터 예방될 수 있고 확진자와 환자도 쉽게 회복될 수 있다", "2상 시험을 통해 효능은 충분히 입증됐다. 효과는 100%", "미국 식품의약국(FDA)에 일반의약품 등록이 돼 있다"고 광고했다. 그는 이 카드가 "코로나19 치료제 혼합 용액의 파동을 디지털화해 출력한 것"이라며 특허 청구를 하기도 했다. 2021년 2월에는 서울 여의도순복음교회 예배에서 담임목사가 이 카드를 ...
한국경제 | 2024.04.29 07:03 | YONHAP
-
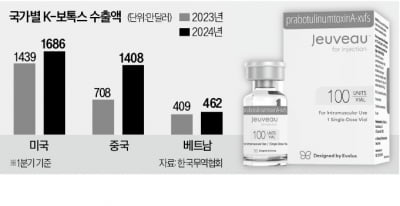
美·中 수출 40% 껑충…날개 단 K-보톡스
... 봤다는 분석이 나온다. 일명 보톡스로 불리는 보툴리눔 톡신의 미국 시장 규모는 6조원(2023년 기준)에 이른다. 미국 보툴리눔 톡신 시장에 처음 진출한 한국 기업은 대웅제약이다. 아시아 기업 최초로 2019년 미국 식품의약국(FDA)의 문턱을 넘었고 현재 파트너사 에볼루스를 통해 ‘나보타’(미국명 주보)를 판매 중이다. 대웅제약 관계자는 “처음 FDA로부터 승인받을 때는 세계 1위 제품인 애브비의 보톡스와 비교임상을 통해 ...
바이오인사이트 | 2024.04.28 17:41 | 남정민
-
美 정부, 11월 대선 앞두고 '멘톨 담배' 금지 결정 연기
... 포함해 아직 더 많은 대화가 필요하다"고 설명했다. 구체적인 일정에 대해서는 언급하지 않았다. 특정한 맛과 향이 나는 가향 담배인 멘톨 담배는 수년 전부터 청소년들의 흡연을 부추긴다는 우려가 제기돼 왔고, 이에 미 식품의약청(FDA)은 2022년 4월 멘톨 담배 등의 판매 금지 방안을 발표했다. 그러나 FDA가 방안을 발표한 지 2년이 지난 시점에 미 당국이 다시 이에 대한 시간이 더 필요하다며 미룬 것이다. 현지 언론은 미 정부의 이번 결정 연기가 대선을 ...
한국경제 | 2024.04.27 06:16 | YONHAP
-
美 암학회 뜬다…HLB·유한양행 강세
... 기대가 사그라들며 주가가 약세를 보인 사례가 많았다. 올해는 10여 개 국내 기업이 ASCO에서 연구 성과를 공개할 예정이다. 특히 시장의 관심을 끄는 기업은 HLB와 유한양행이다. 두 회사 모두 올해 암 신약의 미국 식품의약국(FDA) 승인을 앞두고 있다. 학회에서 발표될 임상 결과가 글로벌 시장 진출의 전초전인 셈이다. 김혜민 KB증권 연구원은 “그동안 고금리 환경에서 제약·바이오 섹터는 시장의 외면을 받았지만 ASCO를 기점으로 기술력을 ...
한국경제 | 2024.04.26 18:40 | 전효성
-
에이비엘바이오 "기술이전 담도암 치료제, 美 패스트트랙 지정"
에이비엘바이오는 파트너사 콤패스 테라퓨틱스(Compass Therapeutics)에 기술이전한 ABL001(CTX-009)이 항암제 파클리탁셀과 담도암에 대한 병용요법으로 미국 식품의약국(FDA)으로부터 패스트트랙 지정을 받았다고 26일 밝혔다. 패스트트랙은 FDA가 개발사의 빠른 신약 개발을 적극적으로 돕기 위해 마련한 제도다. 패스트트랙으로 지정받으면 FDA와 주기적으로 소통할 수 있고, 임상2상 종료 뒤 가속 승인이나 3상 종료 뒤 우선 심사를 ...
한국경제TV | 2024.04.26 17:32