전체뉴스 61-70 / 26,707건
- 최신순
- 정확도순
- 과거순
-
비피도, 상하이 의약품 전시회 참가…글로벌 판로 개척
... 약전(USP)에 등재로 화제가 된 ‘Bifidobaterium bifidum BGN4’를 중심으로 다양한 해외인증을 획득한 자사의 균주를 적극적으로 홍보할 예정이다. 비피도는 자사 균주 3종에 대해 미국 식품의약국(FDA) 신규건강기능식품원료(NDI) 및 원료 안정성(GRAS) 인증을 받았다. 할랄(Halal), 코셔(Kosher) 등의 인증을 획득하며 신규 시장 진출을 위한 준비를 마쳤다. 또한 비피도는 중국 시장 진출을 위해 100% 지분을 ...
바이오인사이트 | 2024.04.09 09:55 | 김유림
-
[해외 통신원 리포트] 일본 DTx의 최근 개발 동향과 임상 전략,그리고 전망
... 미국 아킬리로부터 디지털 치료용 앱 ‘인데버알엑스(EndeavorRx)’의 독점 개발권 및 판매권을 받았다. 이 앱은 소아 주의력결핍과다행동장애(ADHD) 환자의 부주의 증상 개선에 사용하며 미국 식품의약국(FDA)의 승인을 받은 제품이다. SDT-001의 임상 3상은 6~17세 소아 ADHD 환자 164명을 대상으로 진행됐다. ADHD 중증도 평가척도인 ADHD-RS-IV 부주의 점수의 기저치(베이스라인) 대비 변화량을 주요 평가항목으로 삼았다. ...
바이오인사이트 | 2024.04.09 08:49 | 김예나
-
[애널리스트가 만난 CEO] 에이비엘바이오 “4-1BB 이중항체, 베스트 인 클래스 도약… 내년 '이중항체+ADC'도 공개할 것”
... 들었다. 효능 높이고 독성 낮춘 2세대 이중항체 등장할 것 위해주 한국투자증권 연구원(이하 위) 이중항체 시장 변화에 대한 견해가 궁금합니다. 에이비엘바이오 설립 당시에는 암젠의 ‘블린사이토ʼ가 미국 식품의약국(FDA) 승인을 받은 유일한 물질이었습니다. 이후 ‘헴리브라ʼ, ‘콜룸비ʼ까지 총 9종의 이중항체가 FDA 승인을 받았습니다. 이런 성과를 예상하셨나요? 이상훈 에이비엘바이오 대표(이하 이) 당연히 좋은 성과입니다. ...
바이오인사이트 | 2024.04.09 08:43 | 이영애
-
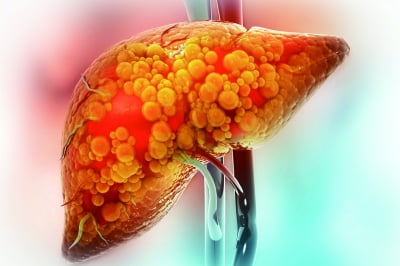
[이슈 분석] MASH 치료제 '레즈디프라' 세계 첫 승인, 차세대 치료제의 패러다임 제시
... 대사이상 관련 지방간질환(Metabolic dysfunction-Associated steatotic Liver Disease)과 달리 간경화, 간암, 간부전 등 심각한 간 질환을 일으킬 수 있는 만성질환이다[그림 1]. 미국 식품의약국(FDA)은 미국에서 약 600만~800만 명의 사람이 중등도에서 진행된 간 섬유증 또는 흉터가 있는 MASH를 앓고 있으며, 환자 수가 가파르게 증가할 것으로 예상하고 있다. 최근 몇 년 동안 MASH는 간 이식의 주요 원인 중 하나가 될 ...
바이오인사이트 | 2024.04.09 08:41 | 김유림
-
[해외 통신원 리포트] 중국 최초의 블록버스터 신약 탄생과 혁신신약의 해외 진출
... 최근까지 15년 동안 산업 전반의 R&D 및 생산 수준의 질적 도약을 달성했다. 이런 질적 도약은 장벽이 높은 고분자 바이오의약품 시장에서 준시바이오사이언스(君实生物)의 ‘토리팔리맙’이 미국 식품의약국(FDA)의 승인을 받으면서 시작됐다. 이는 중국 바이오 혁신기업의 글로벌 진출 서막을 여는 계기가 됐다. 올해 중국 혁신의약품 산업 체인의 해외진출은 ① 상업화(바이오 혁신의약품 및 그 유사체의 유럽과 미국 판매 승인) ② 사업개발(BD)(혁신 ...
바이오인사이트 | 2024.04.09 08:31 | 김예나
-
[2023년 창업도약패키지 선정기업] 알코올, 니코틴 등 중독 관련 디지털치료기기 개발하는 스타트업 '(주)디지털팜'
... 참석을 통해 벤치마킹하거나 기술력을 증대시켜 성장해 나아가고 있다. “미국과 일본, 독일의 공신력 있는 제약회사나 IT 기업들과의 네트워킹을 통해 연구·개발 관련 역량 인프라를 증진하고 있습니다. 미국식품의약국(FDA)에 안전성과 유효성 입증을 위해 미국 할리우드 차병원, 미국UIUC 등과 사용성 평가 협업이 예정돼 있습니다. 청각 재활 디지털 치료제의 미국 FDA 인허가도 추진 예정입니다. 협업이 확정되면 국내 디지털 치료기기 시장에 즉시 침투해 ...
한국경제 | 2024.04.08 22:20 | 이진호
-
엔허투 뛰어넘는 ADC 딜 나오나…'페이로드' 확장이 트렌드
... 특징이다. 지난주 프로파운드바이오를 인수한 덴마크 제약사 젠맙이 대표 사례다. 항체치료제 개발사로 출발한 젠맙은 시젠, 시나픽스, ADC테라퓨틱스 등 글로벌 제약사와 파트너십을 맺고 ADC 신약을 개발해왔다. 미국 식품의약국(FDA) 허가를 받은 자궁경부암 ADC 치료제 '티브닥'도 보유하고 있다. 이번 계약으로 젠맙은 난소암 등 고형암 임상 2상 등 임상개발단계 약물 3개를 추가 확보하게 됐다. GSK도 최대 17억달러를 투자해 ADC 파이프라인을 ...
바이오인사이트 | 2024.04.08 17:14 | 이영애
-
지아이이노베이션, GI-102 피하주사 제형 임상 IND 신청
지아이이노베이션이 차세대 면역항암제 GI-102의 피하주사(SC) 제형 개발을 포함한 임상 1/2상을 위한 임상시험계획(IND) 변경을 식품의약품안전처에 신청했다고 8일 밝혔다. 이번 IND는 피하주사 단독요법 추가 뿐 아니라 기존 순항중인 정맥주사 제형의 화학항암제 등 병용요법 임상 2상 추가에 따른 적응형 임상설계 변경 건이다. 무엇보다 정맥주사와 유사한 약동학을 나타낸 GI-102의 피하주사는 자체 공정개발 노하우를 통해 피하주사 제형...
바이오인사이트 | 2024.04.08 11:45 | 이영애
-
셀트리온 "미국 대형 PBM과 짐펜트라 등재계약 완료"
... 설명했다. 그러면서도 “업체와 협의를 통해 상세한 내용을 알리겠다”고 덧붙였다. 짐펜트라는 셀트리온이 자가면역질환 치료제 램시마를 피하주사(SC)제형으로 개발한 의약품이다. 지난해 10월 미국 식품의약국(FDA)으로부터 신약으로 승인받았다. 셀트리온은 이번 계약에 이미 체결을 완료한 중소형 PBM 계약까지 포함할 경우, 미국 전체 사보험 시장의 40%(가입자 수 기준)를 확보한 것으로 판단한다고 설명했다. 셀트리온 관계자는 “미국 ...
바이오인사이트 | 2024.04.08 11:44 | 남정민
-
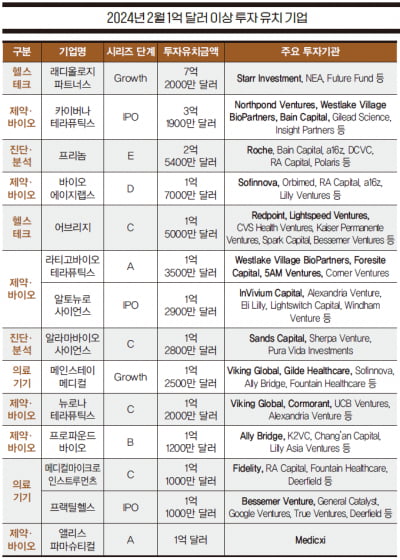
[구영권의 글로벌 바이오헬스케어 투자 브리핑] 래디올로지, 7.2억 달러 유치 카이버나, 3.1억 달러 조달
... 검출할 수 있는 장비와 시약의 상용화를 완료했다. 누적 투자금은 2억2200만 달러다. 메인스테이메디컬(Mainstay Medical) 요통 치료기 ‘ReActiv8’ 개발 회사다. 2021년 미국 FDA로부터 기능적 척추 불안정성과 관련된 기계적 원인이 있는 만성 요통 환자의 하위 집단을 대상으로 ReActiv8의 허가를 받았다. 이번 투자는 바이킹글로벌과 글라이드헬스케어가 주도했다. 누적 투자금은 4억 달러다. 뉴로나테라...
바이오인사이트 | 2024.04.08 09:07 | 안대규